BACITRACIN
Bacitracinum
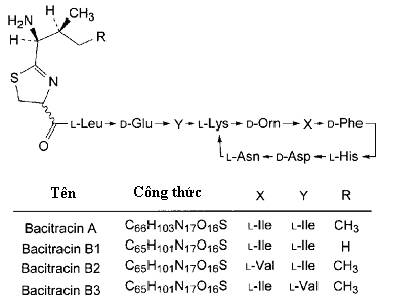
Bacitracin là hỗn hợp
các
polypeptid kháng khuẩn được tạo ra bởi
một số loại Bacillus
licheniformis hoặc Bacillus
subtilis, thành phần chủ yếu là bacitracin A, B1,
B2 và B3. Nó phải chứa ít nhất 60 IU/mg
(tính theo chế phẩm đã làm khô).
Tính chất
Bột trắng hoặc
gần như trắng. Hút ẩm. Dễ tan trong
nước và trong ethanol.
Định tính
Có thể chọn một trong
hai nhóm định tính sau:
Nhóm I: B, C.
Nhóm II: A, C.
A.
Phương pháp sắc
ký lớp mỏng (Phụ lục 5.4)
Bản
mỏng: Silica
gel (TT)
Dung
môi khai triển: Acid acetic băng – nước – butanol (1 : 2
: 4)
Dung
dịch thử: Hòa tan 10 mg chế
phẩm trong dung dịch acid hydrocloric 0,1 N (TT) và
pha loãng thành 1,0 ml với cùng dung môi.
Dung
dịch đối chiếu: Hòa tan 10
mg bacitracin kẽm chuẩn (ĐC)
trong dung dịch acid hydrocloric 0,1 N (TT) và pha
loãng thành 1,0 ml với cùng dung dịch.
Cách
tiến hành: Chấm riêng biệt lên
bản mỏng 10 ml
mỗi dung dịch. Triển khai sắc ký đồ cho
đến khi dung môi đi được một khoảng
bằng ½ chiều dài bản mỏng. Sấy khô bản
mỏng ở 100 oC đến 105 oC. Phun lên
bản mỏng dung dịch
ninhydrin (TT) và sấy ở 110 oC trong 5 phút. Các
vết trên sắc ký đồ của dung dịch thử
có vị trí, kích thước và màu sắc tương
tự các vết trên sắc ký đồ của dung
dịch đối chiếu.
B.
Chế phẩm phải
đáp ứng yêu cầu Phép thử thành phần cấu trúc.
Thành phần
cấu trúc
Phương pháp sắc ký lỏng (phụ lục 5.3). Dùng cách tiến hành chuẩn hóa diện tích pic. Điều chế các dung dịch ngay trước khi dùng.
Pha
động: Lấy 520 thể tích methanol (TT), 40 thể tích acetonitril (TT) và 300 thể tích nước cho vào 100 thể tích dung dịch dikali hydrophosphat (TT) (34,8 g/l)
đã điều chỉnh pH tới 6,0 bằng dung dịch
kali dihydrophosphat (TT) (27,2 g/l).
Dung
dịch thử: Hòa tan 0,100 g chế
phẩm trong 50,0 ml pha động.
Dung
dịch đối chiếu (1): Lắc
20,0 mg bacitracin kẽm chuẩn (ĐC) trong nước.
Thêm 0,2 ml dung dịch acid hydrocloric loãng (TT) và pha loãng
bằng nước thành 10,0 ml.
Dung
dịch đối chiếu (2): Pha
loãng 5,0 ml dung dịch thử với pha động thành
100,0 ml.
Dung
dịch đối chiếu (3): Pha
loãng 1,0 ml dung dịch đối chiếu (2) bằng pha
động thành 10,0 ml.
Dung
dịch đối chiếu (4): Hòa
tan 50,0 mg chế phẩm trong 25,0 ml dung dịch Trilon B (TT)
(40 g/l) đã được
điều chỉnh tới pH 7,0 bằng dung dịch natri hydroxyd loãng (TT). Đun trong nồi
cách thủy đang sôi 30 phút. Để nguội đến
nhiệt độ phòng.
Dung
dịch mẫu trắng: Dung
dịch Trilon B (TT) (40 g/l)
đã được điều chỉnh đến pH 7,0
bằng dung dịch natri hydroxyd
loãng (TT).
Điều
kiện sắc ký:
Cột (25 cm ´ 4,6
mm), chất nhồi end-capped octadecylsilyl silica gel dùng cho
sắc ký (5 mm).
Tốc độ dòng: 1,0
ml/phút.
Detector quang phổ tử
ngoại đặt ở bước sóng 254 nm.
Thể tích tiêm: 100 ml.
Thời gian chạy sắc ký:
Gấp 3 lần thời gian lưu của bacitracin A
Cách tiến hành:
Tiêm mẫu trắng, dung
dịch thử và dung dịch đối chiếu (1) và (3)
Thời gian lưu tương
đối: Tính theo bacitracin A (thời gian lưu từ 15
phút đến 25 phút): bacitracin B1 khoảng 0,6;
bacitracin B3 khoảng 0,8; tạp chất E khoảng
2,5.
Nếu cần, điều
chỉnh thành phần pha động bằng cách thay
đổi thể tích dung môi hữu cơ nhưng vẫn
giữ nguyên tỷ lệ methanol và acetonitril.
Tính thích hợp của hệ
thống:
Tỷ số pic - khe
(peak-valley) tối thiểu 1,2 khi Ho = chiều cao
trên đường nền của pic do bacitracin B1
và Hv = chiều cao trên đường nền
của điểm thấp nhất của đường
cong tách pic này khỏi pic của bacitracin B2. (Trên sắc
ký đồ dung dịch đối chiếu (1))
Giới
hạn: Bacitracin A tối thiểu
40,0%; tổng bacitracin A, B1, B2 và B3
tối thiểu 70,0%.
Bỏ qua các pic tương ứng
với các pic của dung môi mẫu trắng và bỏ qua các
pic có diện tích nhỏ hơn hoặc bằng diện tích
pic của bacitracin A trên sắc ký đồ của dung
dịch đối chiếu (3) (0,5%).
C.
Nung 0,2 g chế phẩm.
Cắn còn lại không đáng kể, nó không có màu vàng ở
nhiệt độ cao. Để
nguội. Hòa tan cắn trong 0,1
ml dung dịch acid hydrocloric loãng
(TT). Thêm 5 ml nước và
0,2 ml dung dịch natri hydroxyd
đặc (TT). Không tạo tủa trắng.
Độ
trong của dung dịch
Dung
dịch S:
Hòa tan 0,25 g chế phẩm trong nước không có carbon dioxyd (TT), pha loãng thành 25 ml với cùng dung mội. Dung dịch S phải trong (Phụ lục 9.2)
pH
(Phụ lục 5.9)
Từ 6,0 đến 7,0 (dùng dung dịch S để thử).
Các peptid liên
quan
Phương pháp sắc ký lỏng hiệu năng cao (Phụ lục 4.3) như mô tả trong “phép thử về thành phần”.
Giới hạn: Tổng diện tích tất cả các pic xuất hiện trước pic bacitracin B1, không được lớn hơn 20,0%.
Tạp
chất E
Phương pháp sắc ký lỏng hiệu năng cao (Phụ lục 4.3) như mô tả trong mục thành phần cấu trúc.
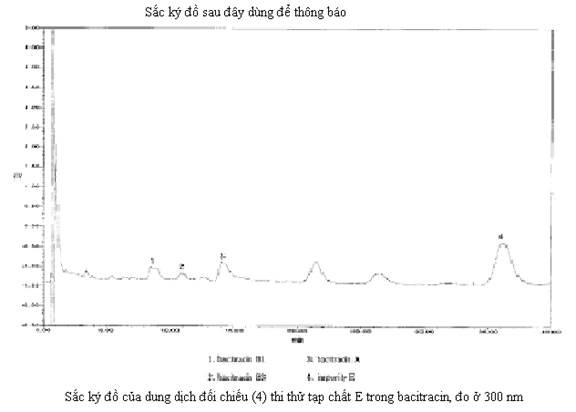
Detector quang phổ đặt ở bước sóng 300 nm đối với dung dịch đối chiếu (4) để xác định pic của tạp chất E..
Tiêm dung dịch thử và dung dịch đối chiếu (2) và (4).
Giới hạn: Trên sắc ký đồ của dung dịch thử, pic của tạp chất E không quá 1,2 lần diện tích pic chính trên sắc ký đồ của dung dịch đối chiếu (2) (6,0%).
Mất
khối lượng do làm khô
Không quá 5,0% (Phụ lục 9.6).
(1,000 g, 60 oC, phospho pentoxyd (TT), áp suất không quá 0,1 kPa, 3 giờ).
Tro sulfat
Không quá 1,0% (Phụ lục 7.7).
Dùng 1,0 g chế phẩm để xác định.
Độ vô
khuẩn
Nếu chế phẩm dự định để điều chế thuốc nhỏ mắt mà không hấp tiệt trùng khi pha chế thì phải đạt độ vô khuẩn (Phụ lục 13.7).
Nội
độc tố vi khuẩn
Không quá 0,8 IU/mg (Phụ lục 13.2) nếu định dùng chế phẩm pha thuốc nhỏ mắt mà không tiến hành loại trừ nội độc tố khi pha chế.
Định
lượng
Tiến hành định lượng kháng sinh bằng phương pháp vi sinh (Phụ lục 13.9). Dùng bacitracin kẽm chuẩn làm chất đối chiếu.
Bảo
quản
Đựng trong bao bì kín, để ở 2 oC đến 8 oC. Nếu chế phẩm vô khuẩn, bảo quản trong bao bì kín, vô khuẩn.
Loại
thuốc
Kháng khuẩn
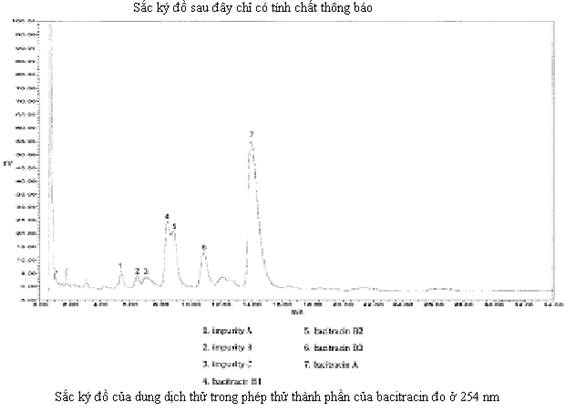
Sau đây là các sắc ký đồ có tính thông báo.
Ghi chú:
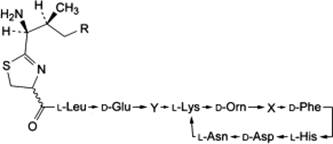
Tạp chất A: X = L-Val, Y = L-Ile, R = H
(bacitracin C1)
Tạp chất B: X = L-Ile, Y = L-Val, R = H
(bacitracin C2)
Tạp chất C: X = Y = L-Val, R = CH3 (bacitracin C3)
Tạp chất D: X = Y = L-Val, R = H
(bacitracin E)
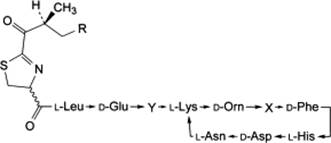
Tạp chất E: X = Y = L-Ile, R = CH3
(bacitracin F)
Tạp chất F: X = Y = L-Ile, R = H
(bacitracin H1)
Tạp chất G: X = L-Val, Y = L-Ile, R = CH3
(bacitracin H2)
Tạp chất H: X = L-Ile, Y = L-Val, R = CH3
(bacitracin H3)
Tạp chất I: X = L-Val, Y = L-Ile, R = H
(bacitracin I1)
Tạp chất J: X = L-Ile, Y = L-Val, R = H
(bacitracin I2)
Tạp chất K: X = Y = L-Val, R = CH3 (bacitracin I3)