CLARITHROMYCIN
Clarithromycinum
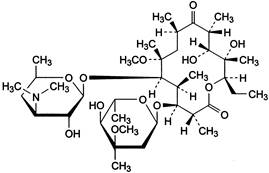
C38H69NO13 P.t.l: 748,0
Clarithromycin
là (3R,4S,5S,6R,7R,9R,11R,12R,13S,14R)-4-[(2,6-Dideoxy-3-C-methyl-3-O-methyl-α-L-ribo-hexopyranosyl)oxy]-14-ethyl-12,13-dihydroxy-7-methoxy-3,5,7,9,11,13-hexamethyl-6-[[3,4,6-trideoxy-3-(dimethylamino)-β-D-xylo-hexopyranosyl]
oxy] oxacyclotetradecan-2,10-dion (6-O-methylerythromycin A), phải chứa từ 96,0 mg đến 102,0% C38H69NO13
tính theo chế phẩm đã làm khô.
Tính
chất
Bột kết tinh màu trắng
hoặc gần như trắng. Thực tế không tan trong
nước, tan trong aceton và methylen clorid, khó tan trong methanol.
Định
tính
Phổ
hồng ngoại (Phụ lục 4.2) của chế phẩm
phải phù hợp với phổ hồng ngoại của clarithromycin chuẩn (ĐC).
Độ
trong và màu sắc của dung dịch
Dung dịch
S:
Hòa tan 0,500 g chế phẩm trong methylen
clorid (TT), pha loãng thành 50,0 ml với cùng dung môi.
Dung
dịch S phải trong hoặc không được đục
hơn hỗn dịch chuẩn đối chiếu số
II (Phụ lục 9.2) và không được đậm màu hơn
dung dịch màu mẫu V7 (Phụ lục 9.3).
Góc quay cực riêng
Từ -94o đến -102o, tính theo chế phẩm
đã làm khô (Phụ lục 6.4).
Dùng dung dịch S.
Tạp chất liên quan
Phương pháp sắc ký lỏng hiệu năng cao (Phụ lục 5.3).
Pha động A: Dung dịch có chứa kali
dihydrophosphat 0,476%, điều chỉnh pH đến 4,4 bằng
dung dịch acid phosphoric loãng
(TT) hoặc bằng dung
dịch kali hydroxyd 4,5% (TT). Lọc qua màng lọc C18.
Pha động B: Acetonitril
(TT).
Dung dịch thử: Hòa tan 75,0 mg chế phẩm trong 25 ml acetonitril (TT), pha loãng thành 50,0
ml với nước.
Dung dịch đối
chiếu (1): Hòa tan
khoảng 75,0 mg clarithromycin chuẩn
(ĐC) trong 25 ml acetonitril
(TT), pha loãng thành 50,0 ml với nước.
Dung dịch đối
chiếu (2): Pha loãng
5,0 ml dung dịch đối chiếu (1) thành 100,0 ml với
hỗn hợp đồng thể tích của acetonitril (TT) và nước.
Dung dịch đối chiếu (3): Pha loãng 1,0 ml dung dịch
đối chiếu (2) thành 10,0 ml với hỗn hợp đồng
thể tích của acetonitril (TT)
và nước.
Dung dịch đối
chiếu (4): Hòa tan
khoảng 15,0 mg hỗn hợp
các tạp chuẩn của clarithromycin (ĐC) trong 5,0 ml acetonitril (TT), pha loãng thành 10,0
ml với nước.
Dung dịch mẫu
trắng: Pha loãng 25,0
ml acetonitril (TT) thành 50,0 ml
với nước, trộn
đều.
Điều kiện sắc ký
Cột thép không gỉ (10 cm x 4,6 mm) được
nhồi pha tĩnh là octadecylsilyl silicagel (3,5 mm). Duy trì nhiệt độ cột ở
40 oC.
Detector quang phổ tử ngoại đặt ở bước
sóng 205 nm.
Thể tích tiêm: 10 ml.
Tốc độ dòng: 1,1 ml/phút với chương trình dung môi:
|
Thời gian (phút) |
Pha động A (% tt/tt) |
Pha động B (% tt/tt) |
|
0 - 32 |
75 → 40 |
25 → 60 |
|
32 - 34 |
40 |
60 |
|
34 - 36 |
40 ® 75 |
60 ® 25 |
|
36 - 42 |
75 |
25 |
Cách tiến hành: Tiến hành sắc ký với dung dịch
thử, dung dịch đối chiếu (2), (3) và (4).
Độ lưu giữ tương đối (r): Độ lưu giữ tương đối so với clarithromycin (thời gian lưu khoảng 11 phút) của tạp chất I khoảng 0,38; của tạp chất A khoảng 0,42; của tạp chất J khoảng 0,63; tạp chất L khoảng 0,74; tạp chất B khoảng 0,79; tạp chất M khoảng 0,81; tạp chất C khoảng 0,89; của tạp chất D khoảng 0,96; của tạp chất N khoảng 1,15; của tạp chất E khoảng 1,27, tạp chất F khoảng 1,33; tạp chất P khoảng 1,35; tạp chất O khoảng 1,41; tạp chất K khoảng 1,59; tạp chất G khoảng 1,72 và tạp chất H khoảng 1,82.
Độ thích hợp của hệ thống:
Hệ số đối xứng: Không được quá 1,7 đối với píc của clarithromycin trên sắc ký đồ của dung dịch đới chiếu (2).
Tỷ số peak-Valley (HP/HV): Ít nhất phải bằng 3,0 (tỷ số này được áp dụng để đánh giá độ thích hợp hệ thống trong phép thử tạp chất liên quan, khi 2 píc không tách hoàn toàn tới chân đường nền). HP là chiều cao tính từ đường nền của píc tạp chất D; HV là chiều cao tính từ đường nền đến điểm thấp nhất của đường cong phân tách giữa píc tạp chất D và píc của clarithromycin trên sắc ký đồ dung dịch đối chiếu (4).
Giới hạn:
Hệ số hiệu chỉnh: Để tính toán hàm lượng các tạp chất, nhân diện tích píc của các tạp chất sau với hệ số hiệu chỉnh tương ứng. Tạp chất G có hệ số hiệu chỉnh bằng 0,27; tạp chất H có hệ số hiệu chỉnh bằng 0,15. Dùng dung dịch đối chiếu (4) để xác định píc của tạp chất G và H.
Từng tạp chất có diện tích píc không được
lớn hơn 2 lần diện tích píc chính của dung
dịch đối chiếu (3) (1,0%) và không được
có quá 4 píc tạp chất lớn hơn 0,8 lần diện
tích píc chính của dung dịch đối chiếu (3) (0,4%).
Tổng diện tích các píc tạp chất không được
lơn hơn 7 lần diện tích píc chính của dung
dịch đối chiếu (3) (3,5%).
Bỏ qua các píc có diện tích nhỏ hơn 0,2 lần
diện tích píc chính của dung dịch đối chiếu
(3) (0,1%). Bỏ qua các píc rửa giải ra trước
tạp chất I và các píc rửa giải ra sau tạp
chất H.
Ghi chú:
Tạp
chất A: Clarithromycin F
Tạp
chất B: 6-O-methyl-15-norerythromycin A
Tạp
chất C: 6-O-methylerythromycin A (E)-9-oxim
Tạp
chất D: 3’’-N-demethyl-6-O-methylerythromycin A
Tạp
chất E: 6,11-di-O-methylerythromycin A
Tạp
chất F: 6,12-di-O-methylerythromycin A
Tạp
chất G: (6-O-methylerythromycin A (E)-9-(O-methyloxim)
Tạp
chất H: 3’’-N-demethyl-3’-N-formyl-6-O-methylerythromycin
A
Tạp
chất I: 3-O-decladinosyl-6-O-methylerythromycin A
Tạp
chất J: Erythromycin A (E)-9-oxim
Tạp
chất K: (1S,2R,5R,6S,7S,8R,9R,11Z)-2-ethyl-6-hydroxy-9-methoxy-1,5,7,9,11,13-hexamethyl-8-[[3,4,6-trideoxy-3-(dimethylamino)-β-D-xylo-hexopyranosyl]oxy]-3,15-dioxabicyclo[10.2.1]pentadeca-11,13-dien-4-on
(3-O-decladinosyl-8,9:10,11-dianhydro-6-O-methylerythromycin
A-9,12-hemiketal
Tạp
chất L: 6-O-methylerythromycin A (Z)-9-oxim
Tạp
chất M: 3’’-N-demethyl-6-O-methylerythromycin A (E)-9-oxim
Tạp
chất N: (10E)-10,11-didehydro-11-deoxy-6-O-methylerythromycin
A
Tạp
chất O: 6-O-methylerythromycin A (Z)-9-(O-methyloxim
Tạp
chất P: 4’,6-di-O-methylerythromycin A
Kim loại nặng
Không được quá 20 phần triệu (Phụ
lục 9.4.8)
Hòa tan 1,0 g chế phẩm trong hỗn hợp nước - dioxan (15 : 85), pha
loãng thành 20 ml với cùng dung môi. Lấy 12 ml dung dịch thu được
tiến hành thử theo phương pháp 2. Dùng dung dịch chì mẫu 100 phần
triệu (TT) pha loãng với hỗn hợp nước - dioxan (15 : 85) để
chuẩn bị mẫu đối
chiếu 1 phần triệu.
Nước
Không được quá 2,0% (Phụ lục 10.3)
Dùng 0,500 g chế
phẩm.
Tro sulfat
Không quá 0,2% (Phụ lục 9.9,
phương pháp 2).
Dùng 0,5 g chế phẩm.
Định lượng
Phương pháp sắc ký lỏng hiệu năng cao (Phụ lục 5.3), điều kiện sắc ký giống như ở phần thử tạp chất liên quan.
Tiến hành sắc ký với dung dịch thử và dung
dịch đối chiếu (1), từ diện tích píc
đáp ứng của clarithromycin trên sắc ký đồ
của dung dịch thử và dung dịch đối
chiếu (1), tính toán hàm lượng C38H69NO13.
Bảo quản
Đựng trong đồ bao gói kín, tránh ánh sáng.
Nhãn
Phải quy định rõ thời hạn sử
dụng và điều kiện bảo quản.
Loại thuốc
Kháng khuẩn.
Chế phẩm
Viên nén, nang, bột pha hỗn dịch uống.